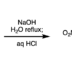镍催化的惰性C–H键直接偶联反应的开发和机理阐明
Today:0views / Total:3,966views

利用镍催化的有机合成反应,首先能想到的就是1972年报道的Kumada—Tamao—Corriu(熊田-玉尾-Corriu)偶联反应,在镍的催化下,芳香卤化物与有机金属反应剂(Grignard反应剂)之间发生偶联反应,生成芳香族化合物的衍生物。镍催化的Kumada-Tamao-Corriu偶联反应是所有偶联反应中最早被开发出来的反应,而现在,却被反应适用性更高,属于周期表同族的金属钯催化剂作为主流研究,钯催化的偶联反应研究也因为在医药、有机光电材料的广泛应用而授予诺贝尔奖。然而,镍催化与钯催化剂相比,价格低廉,对于各类惰性C–O键、C–C键的氧化加成反应具有更好活性,近些年来,化学研究者利用镍催化剂的这些特性,相继报道了新型偶联反应,由钯催化剂很难实现的反应, 镍催化剂再次成为研究关注热点。
另外,我们还不使用对空气、水等不稳定的金属有机反应试剂,而是将这些芳香化合物的惰性C–H键无需金属活化阶段,直接转变偶联的「C–H键偶联反应」,这也是目前大多数合成化学家们一起努力并慢慢完善的有机化学新潮流3,4,5)。而我们,也在C–H键活化偶联的研究中,开发了许多促进反应的分子催化剂,并会一直致力于这一目标,为该领域的丰富完善做出贡献。
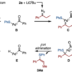
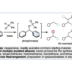
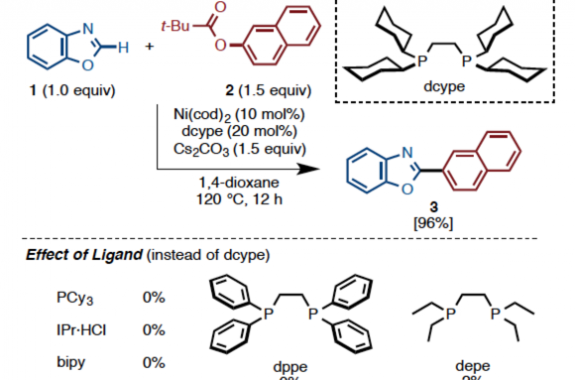
作为我们在该领域的代表性研究之一,是研究课题组在2009年发表的镍催化的1,3-azole类的C–H键和芳香卤化物的直接偶联反应6,7,8)。镍催化的C–H键偶联反应虽然是世界上最早实现的,不过除了镍价格低廉以外,其他的优势并不突出。而将镍催化剂的特点用于钯催化剂难以实现的某些特殊芳香环试剂的偶联反应中,是我们的开发的反应特点和日后研究方向之一。在这里,就为大家介绍我们曾经开发出的镍催化直接偶联反应,特别是为什么这些反应会进行等,会从这些具体方面来阐述。


 日本語
日本語 English
English